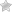Синдром Нельсона – это эндокринное заболевание, которое развивается как следствие двусторонней адреналэктомии или длительной терапии митотаном. Характеризуется формированием и/или ростом аденомы гипофиза, избыточным производством АКТГ, хронической недостаточностью коры надпочечников (ХНН). Специфический симптом – патологическая пигментация слизистых оболочек, кожи. Наблюдается слабость, адинамия, артериальная гипотензия, тошнота, боли в костях, потеря зрения, утрата обоняния, снижение памяти, эмоциональная лабильность. Диагноз устанавливается на основании анамнеза, результатов анализа на АКТГ, данных МРТ (КТ) головного мозга. Лечение комплексное: хирургическое, лучевое, медикаментозное.
Синдром Нельсона получил свое название по фамилии врача-исследователя из США Д. Нельсона.
В 1950-х годах он вместе с коллегами описал клинический случай женщины, у которой спустя несколько лет после двустороннего удаления надпочечников сформировалась опухоль гипофиза.
К 1960 году данные были накоплены и систематизированы, а синдром выделен как отдельная нозологическая единица. В последние десятилетия распространенность патологии сокращается, что связано с уменьшением количества адреналэктомий.
Среди пациентов с удаленными надпочечниками эпидемиология составляет 5-10%. Заболевание диагностируется после хирургического вмешательства, временной промежуток между операцией и появлением симптоматики колеблется от 3-6 месяцев до 20-25 лет. Наиболее высокий риск отмечается в течение первых 6 лет.
Синдром Нельсона
Сбои в работе гипоталамо-гипофизарной системы обусловлены утратой тормозящего влияния кортикоидных гормонов на клетки аденогипофиза, синтезирующие адренокортикотропин. Синдром Нельсона возникает при абсолютном выпадении функции коры надпочечников в результате лечения болезни Иценко-Кушинга. Причинами могут быть:
- Двусторонняя адреналэктомия. Хирургическое удаление двух надпочечников – наиболее распространенный фактор возникновения синдрома. Выработка кортикостероидов прекращается, синтез АКТГ значительно увеличивается.
- Односторонняя адреналэктомия, терапия митотаном. Реже патология развивается после удаления одного надпочечника, на фоне угнетения функций второго препаратами группы ингибиторов синтеза стероидов. Патологические процессы аналогичны таковым при билатеральной адреналэктомии, но медленнее прогрессируют.
- Длительное лечение митотаном. Препарат относится к противоопухолевым средствам, ингибиторам производства гормонов надпочечников. Он разрушает опухолевую и нормальную ткань надпочечниковой коры. При длительном приеме возможна полная утрата гормоносекретирующей функции.
Не все пациенты с дисфункцией надпочечников страдают от синдрома Нельсона.
Его формированию способствует ряд факторов, в том числе – высокая секреция кортизола до терапии, доброкачественное новообразование гипофиза, молодой возраст больных к моменту адреналэктомии.
Пик заболеваемости приходится на 26 лет, после 40 лет риск приближается к нулю. Вероятность синдрома более низка у пациентов, перенесших оперативное вмешательство на гипофизе.
Ключевые патогенетические процессы синдрома Нельсона – недостаток ингибирующего влияния кортизола на АКТГ-производящие клетки, возобновление роста и быстрое прогрессирование гипофизарной опухоли, сформировавшейся при болезни Кушинга.
После резекции надпочечников или при продолжительном приеме митотана нарушается физиологическая регуляция функций надпочечников гипоталамо-гипофизарным комплексом.
Это ведет к значительному повышению количества АКТГ, формированию гипофизарной аденомы.
Усиление пигментации объясняется вненадпочечниковым воздействием АКТГ на меланоциты – клетки кожи, производящие пигмент мелатонин черно-коричневого и желто-красного цвета.
Кроме этого, гормон стимулирует липолиз и секрецию инсулина, оказывая гипогликемический эффект.
У лиц с синдромом Нельсона он усиливает метаболизм кортикоидных гормонов, поэтому для устранения признаков надпочечниковой недостаточности требуется назначение высоких доз их синтетических аналогов.
Клиническая картина включает прогрессирующую гиперпигментацию кожи, симптомы наличия АКТГ-продуцирующей опухоли и ХНН, расстройства со стороны ЦНС и органов зрения, связанные с увеличением размеров аденомы. Гиперпигментация проявляется как потемнение открытых участков и областей, подверженных трению: лица, шеи, кистей рук, подмышечных впадин, мест посадки брюк и воротника.
Окрашивается полость рта и область анального отверстия. Наиболее яркая пигментация характерна для послеоперационных швов. Цвет варьируется от светлого загара до темно-коричневого с фиолетовым оттенком, напрямую коррелирует с концентрацией АКТГ и бета-липотропина.
Меланодермия становится менее выраженной при адекватной гормонозаместительной терапии, усиливается при обострении заболевания.
Надпочечниковая недостаточность склонна к декомпенсации, реализуется через малые и большие кризы. При малом кризе пациенты чувствуют слабость и суставные боли, теряют аппетит.
Часто возникают приступы артериальной гипотензии, головокружения и обмороки. При большом кризе резко нарастает тошнота, появляется рвота, диарея, абдоминальные и мышечные боли.
Тахикардия и артериальная гипотония более выраженные, стойкие. Температура тела поднимается до 39° C.
Прогрессивный рост кортикотропиномы проявляется нейроофтальмологической симптоматикой. Наиболее характерен хиазмальный синдром: сужение границ поля зрения в верхневисочном или нижневисочном квадранте, выпадение половин полей зрения.
Позже изменяется состояние глазного дна, снижается острота зрения, развивается слепота. Психоневрологический статус характеризуется нарастанием астено-депрессивных и астено-фобических состояний.
Больные становятся эмоционально неустойчивыми, тревожными, мнительными, часто пребывают в подавленном настроении.
При отсутствии лечения кортикотропинома увеличивается, повышается риск спонтанного внутриопухолевого кровоизлияния, провоцирующего односторонний паралич глазодвигательного нерва (офтальмоплегии). Большие аденомы сдавливают окружающие области и потенцируют разнообразные неврологические нарушения.
Антеселлярное распространение новообразования приводит к патологии обоняния и психическим расстройствам; параселлярное – к поражению III, IV, V и VI пар черепно-мозговых нервов: нарушаются глазодвигательные функции, страдают различные виды чувствительности лица.
При росте опухоли вверх возникают общемозговые симптомы – помрачение сознания, головная боль, головокружение, рвота, генерализованные судорожные приступы.
Врач-эндокринолог проводит клинический опрос и осмотр больного, собирает анамнестические данные. Диагноз синдрома Нельсона основывается на наличии характерных симптомов, предшествующей болезни Кушинга и тотальной адреналэктомии.
Дифференциальная диагностика требует разграничения данного синдрома с болезнью Аддисона и синдромом Кушинга, сопровождающегося повышением АКТГ из-за развития эктопированной опухоли.
Для подтверждения диагноза необходимо подтвердить гиперсекрецию АКТГ, присутствие опухоли в гипофизе. Используются следующие методы:
- Анализ крови на АКТГ. При кортикотропиноме и утрате функции надпочечников концентрация АКТГ в крови составляет 200 пг/мл и более, отсутствует циркадный ритм секреции гормона – показатели анализа относительно стабильны днем и ночью. Они отражают активность неоплазии и напрямую коррелируют с выраженностью гиперпигментации. Коричневая, черно-фиолетовая окраска сопровождается повышением уровня АКТГ до 1000 пг/мл; легкая и умеренная гиперпигментация в операционных швах и областях частого трения – до 200-400 пг/мл.
- МРТ головы. Визуализация микроаденом затруднена, поскольку они зачастую располагаются в турецком седле и не изменяют его структуру. При небольших размерах опухоли турецкое седло соответствует норме либо незначительно увеличено, пристальное изучение боковых проекций позволяет определить наличие новообразования. Большие и средние аденомы более заметны – седло увеличено, стенки истончены или разрушены. При крупных неоплазиях обнаруживается расширенный вход в турецкое седло, укороченные клиновидные отростки. МРТ гипофиза может быть заменена рентгенографией турецкого седла, но данные будут менее точны. Для получения дополнительной информации об аденоме проводится КТ.
- Нейроофтальмологическое обследование. При прогрессивном увеличении опухоли диагностируются изменения в глазном дне, выпадения наружных полей и снижение остроты зрения, опущение верхнего века. На ЭЭГ выявляются признаки, указывающие на повышенную активацию гипоталамуса – регистрируется высокоамплитудный альфа-ритм распространяющийся по всем отведениям. Быстрый рост опухоли провоцирует разряды тета-волн, больше выраженные во фронтальных отведениях. Общее повышение биоэлектроактивности мозга подтверждает усиление гипоталамо-гипофизарных процессов.
Терапия направлена на удаление или подавление активности кортикотропиномы, компенсацию ХНН. Для достижения положительного результата и предупреждения рецидивов используются комбинированные методы лечения, включающие следующие процедуры в различных сочетаниях:
- Прием медикаментов. Медикаментозная коррекция целесообразна при новообразовании, которое не выходит за пределы турецкого седла, при рецидиве синдрома. Используются препараты, снижающие уровень АКТГ: серотониновые блокаторы, стимуляторы дофаминовых рецепторов. Для компенсации ХНН проводится заместительная терапия минерало- и глюкокортикоидами.
- Радиационная терапия. Курс процедур рекомендуется пациентам с аденомами маленьких размеров, а также после проведения резекции опухоли, при рецидивах синдрома. Применяется методика облучения γ-лучами и протонными пучками, введения в ткани гипофиза радиоактивных изотопов иттрия и серебра.
- Хирургическая операция. Метод показан при аденомах маленьких, средних и больших размеров. Микрохирургическое оборудование позволяет полностью удалить образование, но не исключает развития рецидива, поэтому после оперативного вмешательства назначается курс лучевого лечения.
- Криотерапия. Низкотемпературный метод воздействия эффективен при опухолях небольших размеров. Жидкий азот стереотаксически через трансназальный транссфеноидальный доступ подводится к аденоме и разрушает ее ткани.
Исход заболевания благоприятный при медленном росте опухоли, ее успешном удалении, достижении компенсации ХНН. В таких случаях состояние пациентов остается стабильным, вероятность рецидива невелика.
В качестве профилактической меры больным, перенесшим билатеральную адреналэктомию, рекомендуется ежегодно назначать обследования, которые позволяют визуализировать область расположения гипофизарной аденомы, контролировать содержание АКТГ.
Кроме того, пациентам показаны регулярные офтальмологические осмотры.
Источник: https://www.KrasotaiMedicina.ru/diseases/zabolevanija_endocrinology/Nelson-syndrome
Синдром Нельсона
Заболевание, развивающейся в результате двухстороннего удаления надпочечников, и сопровождающейся опухолевыми образованиями в гипофизе головного мозга, называется синдром Нельсона.
Гипофиз — это один из главных органов эндокринной системы, отвечающий за выработку гормонов, он играет огромную роль в жизни человека: отвечает за его рос, метаболизм, а также за жизнедеятельность половых органов и зачатие ребенка.
Поэтому адреналэктомия, то есть удаление надпочечников, и продолжительное лечение метотаном, приводят к росту аденомы, избыточной выработки адренокортикотропного гормона (АКТГ), который регулирует работу этого органа. Кроме этого в результате оперативного вмешательства развивается хроническая недостаточность коры надпочечников.
Содержание
- 1 Симптомы
- 2 Диагностика
- 3 Причины
- 4 Терапия заболевания
- 5 Редактор
Симптомы
Обычно состояние пациента и проявление признаков заболевания зависит от размера новообразования в гипофизе, и его влияния на эндокринную систему человека. Как правило, сбои в организме могут проявляться характерными признаками:
- Обширной пигментацией всего тела и слизистых оболочек.
- Отмечается общая слабость организма.
- Развивается артериальная гипотензия. Появляется тошнота.
- Также отмечается болевой синдром в костях.
- Нередко снижается зрение, память, утрачивается обоняние, нарушается эмоциональный фон человека, приводящие к развитию депрессии и стрессов.
- Пациент теряет аппетит, что приводит к снижению веса.
- Могут отмечаться параличи различной степени тяжести.
Один из симптомов синдрома Нельсона. Источник: meduniver.com
Чрезмерная пигментация носит стабильный характер на всем протяжении развития патологии. Особенно сильно она может выражаться в районе соприкосновения тела с одеждой: подмышками, на шее, в области пояса.
Поэтому пациентам, которым проведено удаление надпочечников, ни в коем случае нельзя игнорировать указанные симптомы, в противном случае это может привести к опасным осложнениям, а то и потери жизни.
Диагностика
Как правило, диагностируется заболевание в основном в молодом возрасте пациента от 26 и до 40 лет, спустя много лет после удаления надпочечников. Колебаться этот диапазон может от нескольких месяцев и до 20-25 лет, однако в основном самый большой риск возникновения опухолей в шесть лет.
Диагноз устанавливается на основании составления анамнеза, прохождения МРТ и КТ головного мозга, а также данных анализов на наличие гормона АКТГ. Во время беседы с пациентом доктор изучает возможность предрасположенности к этому заболеванию. То есть, само протекание болезни Иценко-Кушинга (избыточная выработка АКТГ-гормона) и сопутствующая ему операция.
Синдром Нельсона развивается у пациентов с болезнью Кушинга. Источник: medsimptom.org
Кроме этого анализируется внешнее ее проявление. При сопоставлении всех патологических проявлений патологии, можно подтвердить или опровергнуть заболевание. Эндокринолог направляет пациента на прохождение ряда анализов:
- Проводится общий и расширенный анализ крови.
- Исследуется урина.
- Проводится исследование крови на выявление гормонов, то есть определяется уровень АКТГ и кортизола, регулирующего его выработку.
Все это направлено на выявление гормональных нарушений в организме и является наиболее важным при постановке диагноза. При повышении АКТГ, практически всегда диагноз подтверждается. Для более точной диагностики, кроме МРТ и КТ, назначаются и такие инструментальные обследования: электроэнцелография, эфоэнцелоскопия, довольно часто исследуют почки с помощью ультразвуковой диагностики.
Причины
Развитию синдрома Нельсона могут сопутствовать несколько факторов:
- Наиболее распространенной причиной считается удаление сразу двух надпочечников. Так как в этом случае полностью прекращается выработка кортикостероидов, контролирующих быстрый рост АКТГ гормонов.
- При удалении одного надпочечника и лечении метотаном, препаратом способным разрушать не только опухолевые образования, но и здоровые ткани, болезнь продолжает прогрессировать, но значительно медленнее. Длительное этого препарата, может привести к полной утрате функций выработки гормонов.
Пациентам, которым проведено удаление опухоли на гипофиза, развитие синдрома Нельсона снижается во много раз и практически, равна нулю.
Терапия заболевания
Для того, чтобы лечение дало положительные результаты, проводится комплексная терапия, включающая несколько аспектов.
Снижение развития опухоли и синтеза уровня АКТГ в крови, а также стабилизация гормонального уровня, возможна при использовании различных методов терапии.
Сюда включается: прием лекарственных препаратов, удаление опухоли в гипофизе и лучевая терапия на поврежденный участок головного мозга.
Этот метод используется намного чаще других, потому что он наиболее эффективен и дает положительные прогнозы.
Проводится восстановительная терапия деятельности надпочечников с помощью специальных медикаментозных препаратов. Это помогает купировать надпочечниковую недостаточность, устранить симптомы заболевания, а также ускорить лечение.
Какой лучше всего выбрать метод для восстановления организма, будет решать лечащий врач при непосредственном участии эндокринолога. Самолечением нельзя заниматься ни в коем случае, это может способствовать развитию тяжелых осложнений. Правильно организованное лечение и не запущенность заболевания гарантирует оптимистический прогноз.
Однако при этом следует помнить, что это продолжительная терапия, и на скорое выздоровление не приходится рассчитывать. По статистике медицинской практики большинство пациентов остаются нетрудоспособными и в течение оставшейся жизни, им придется постоянно наблюдаться у ряда специалистов, в том числе: эндокринолога, терапевта, окулиста и невропатолога.
Как известно, предупредить заболевание проще, чем лечить последствия развития патологии, поэтому нужно следить за своим здоровьем и регулярно проходить профилактические осмотры.
Источник: https://uran.help/diseases/sindrom-nelsona.html
Синдром Нельсона — симптомы |
В каких случаях у человека может развиться синдром Нельсона? На сегодняшний день это достаточно редкая эндокринная патология, но тем не менее про синдром Нельсона должна быть отдельная публикация на endokrinoloq.ru. Здравствуйте! Из этой статьи вы узнаете, чем чревато двустороннее удаление надпочечников у пациента, получившего ранее диагноз «болезнь Иценко-Кушинга».
Этот синдром может возникнуть и через 2 месяца после оперативного вмешательства, и через 25 лет. Другими словами, сроки развития данной патологии после двусторонней адреналэктомии очень вариабельны, однако у большинства пациентов синдром Нельсона можно наблюдать примерно через 6-8 лет после операции.
Почему возникает синдром Нельсона?
Выше было указано, что синдром Нельсона в последние годы наблюдается очень и очень редко. И это неспроста.
В прошлом, когда медицинская наука еще не была развита как сейчас, существовали достаточно заметные ограничения в методиках ведения больных с гиперкортицизмом гипофизарного генеза (болезнь Иценко-Кушинга).
И именно в те годы синдром Нельсона можно было наблюдать практически у каждого второго больного, некогда перенесшего операцию по удалению обоих надпочечников.
Врачей-хирургов, владеющих совершенными методиками проведения оперативных вмешательств на мозге, можно было посчитать по пальцам. Да и совершенными, согласно современным представлениям, эти методики сейчас называть язык как-то не поворачивается…
В те годы наиболее оптимальным методом лечения такого заболевания, как Иценко-Кушинга, являлось оперативное удаление бригадой хирургов надпочечников с обеих сторон. Делалось это в целях ликвидации практически единственного источника кортикостероидных гормонов, то есть минералокортикоидов и глюкокортикоидов.
И действительно, после такого лечения больной буквально «вставал на ноги» после тяжелого заболевания, поскольку удалялся основной источник синтеза этих гормонов-виновников, уровень которых зашкаливал норму прежде.
И возникало ощущение, что человек выздоровел.
Но если вдуматься… Опухоль гипофиза-то не исчезла. И хотя после операции уже нет в крови избытка кортикостероидов, опухоль гипофиза по-прежнему продолжает активно выделять гормон АКТГ.
К чему же это приводит?
Избыточный синтез АКТГ, не находя мишени для своего действия, приводит к постепенному (или быстро прогрессирующему) росту изначально маленькой опухоли. При этом даже аденома, которая имеет доброкачественный характер, представляет значительную угрозу для жизни больного. Ведь место ее расположения — черепная коробка. Опухоли просто некуда расти!
Поэтому основные симптомы при возникновении синдрома Нельсона связаны со сдавлением и смещением церебральных структур. Естественно, после такой тяжелой операции больному пожизненно нужно будет принимать заместительную гормональную терапию препаратами гормонов надпочечников.
Подбирать дозы этих препаратов — занятие из непростых. Даже у очень опытных и грамотных в этом отношении специалистов могут возникать погрешности в терапии, ведь практически невозможно подстроиться под естественные механизмы регуляции человеческого организма, так что всегда есть риск введения химического препарата меньше требуемой дозы, или же его передозировка.
К большому сожалению, и на сегодняшний день иногда, хоть и очень редко, можно наблюдать развитие этого синдрома у пациентов, например, при тяжелом течении болезни Кушинга.
Как проявляется синдром Нельсона
Симптоматика при синдроме возникает из-за:
- Передозировки гормональных препаратов. При этом отмечаются такие проявления, как артериальная гипертензия, «матронизм» (красное лицо округлой формы), неравномерный тип ожирения, тахикардия, боли в области спины, мышечная слабость, изменения трофики кожи.
- Роста гипофизарной опухоли. Характеризуется снижением обоняния, головными болями, диэнцефальными нарушениями, нарушением зрения, изменением вкусовых ощущений, гиперпигментацией мест трения и открытых частей тела.
- Дефицитом гормонов после операции, которое имеет лабильное течение. Возникающая при этом надпочечниковая недостаточность имеет тенденцию к развитию кризов острой недостаточности. При этом может возникать нарастающая слабость, рвота и тошнота, снижение аппетита, быстрая утомляемость, понижение артериального давления, боли к суставах и костях.
Синдром Нельсона и его лечение
Для того, чтобы не дать возможности развитию этого синдрома после двусторонней адреналэктомии необходимо проведение лучевого облучения области гипофиза.
Если же синдром Нельсона уже имеется, лечение заключается в корректировке назначенных доз гормональных препаратов для заместительного лечения. Помимо этого, осуществляется воздействие на систему гипоталамус-гипофиз (удаление опухоли, лучевая терапия, подавление синтеза АКТГ при помощи определенных медикаментов).
Оставь комментарий, и получи ПОДАРОК!
Поделиться с друзьями:
Источник: http://endokrinoloq.ru/takoj-redkij-sindrom-nelsona
Как проявляется и лечится синдром Нельсона
Синдром Нельсона является своеобразным осложнением терапии болезни Иценко-Кушинга. Возникает чаще через 6 лет с момента двустороннего удаления надпочечных желез. Ему особенно подвержены молодые прооперированные пациенты.
Наличие исходно существующей опухоли является самым важным условием для появления этой патологии. Адренокортикотропный гормон (АКТГ) у пациентов после операции вырабатывается в постоянно высоких количествах, вне зависимости от необходимости в нем, а аденома имеет свойство быстро расти.
Самый первый и типичный признак – это потемнение кожных покровов: открытые участки тела, складки приобретают темно-коричневый цвет с фиолетовым оттенком. Второй –необычно высокая потребность в гормонах для заместительной терапии. С этим связано развитие адреналовых кризов при малейшем перенапряжении или даже на фоне полного благополучия.
Криз бывает относительно легким – нарастает слабость, снижается аппетит, появляется ломота в костях, суставах, снижается давление крови.
Тяжелее протекают внезапные «большие» приступы: тошнота, рвотные позывы; боль в животе, понос; слабость достигает такого уровня, что больной не может двигаться; нарастают мышечные и суставные боли; повышена температура до 40 градусов; обморочные состояния, сосудистый коллапса из-за резкого падения давления.
Осложнения болезни: растущая вверх аденома гипофиза приводит к нарушениям зрения, выпадению боковых полей, снижению четкости предметов, бывает двусторонняя слепота. Если растет вперед, то страдает обоняние и психика, при боковом отекают веки, глазное яблоко смещается кпереди, появляется односторонняя слепота и головная боль.
Прорастание нижних тканей изменяет голос (гнусавый) и затрудняет глотание. Наиболее тяжелый вариант – переход на задние части мозга. У больных обнаруживают признаки стволовых нарушений, патологические рефлексы, глотание становится почти невозможным.
При кровоизлиянии в ткань опухоли появляется резкая головная боль, подает давление, возникает тошнота, рвота, нарушается двигательная активность и чувствительность.
Диагностика начинается с определения концентрации АКТГ. При маленьких размерах аденомы проводят рентгенограмму, КТ. При больших размерах ориентируются на офтальмологические изменения, для которых характерны: изменения на глазном дне, опущение верхнего века, исчезновение боковых полей зрения, частичная или полная слепота.
Опущение верхнего века при синдроме Нельсона
Цели лечения синдрома Нельсона – компенсировать дефицит кортизола, подавить образование АКТГ, предупредить последствия роста опухоли. Есть три направления:
- Медикаментозная терапия – Перитол (антиаллергический препарат, блокатор серотонина), Парлодел (стимулятор дофамина) и Депакин (Конвулекс). Редко используются как основной метод лечения, чаще для послеоперационной профилактики рецидивов
- Лучевая терапия. Облучение может быть проведено дистанционно гамма-лучами и протонами, а также в сам гипофиз вводится радиоактивное золото, которое постепенно разрушает опухоль. Этот способ подходит только для небольших образований. Назначают после оперативного лечения.
- Операция. Если направление роста опухоли идет вниз от гипофиза, то ее лучше удалить при доступе через носовые ходы. При растущих вверх аденомах или крупных новообразованиях применяется трепанация черепа. Положительный результат от удаления чаще бывает при небольших размерах, пока нет признаков сдавления соседних тканей. При больших образованиях даже после удаления не всегда удается полностью восстановить зрения и неврологический статус
Читайте подробнее в нашей статье о синдроме Нельсона, его проявлениях, лечении и прогнозе для больных.
При нехватке какого гормона образуется синдром Нельсона
Это заболевание является своеобразным осложнением терапии болезни Иценко-Кушинга.
Для пациентов, которые страдают от гиперкортицизма (избытка гормонов надпочечников), радикальным способом лечения является двустороннее удаление надпочечных желез.
Через время (чаще 6 лет), даже на фоне гормональной терапии, возникает синдром Нельсона. Ему в особенно подвержены молодые прооперированные пациенты.
Удаление надпочечных желез (адреналэктомия) при болезни Иценко-Кушинга способствует снижению содержания кортизола. В ответ гипофиз усиленно вырабатывает адренокортикотропный гормон (АКТГ). Этот процесс связан с наличием аденомы (кортикотропиномы), которая была у больного еще до операции, но по каким-то причинам не была обнаружена. При дефиците кортизола она активно прогрессирует.
Адреналэктомия
Наличие исходно существующей опухоли является самым важным условием для появления этой патологии. При недостатке гормонов (например, при болезни Аддисона) и отсутствии опухоли подобные нарушения не возникают. АКТГ у пациентов после операции вырабатывается в постоянно высоких количествах, вне зависимости от необходимости в нем, а аденома имеет свойство быстро расти.
Рекомендуем прочитать статью об аденоме гипофиза. Из нее вы узнаете о причинах появления аденомы гипофиза, симптомах опухоли головного мозга у мужчин и женщин, классификации болезни, а также о диагностике и лечении аденомы гипофиза.
А здесь подробнее об операции аденомы гипофиза.
Симптомы патологии
Самый первый и типичный признак – это потемнение кожных покровов. При концентрации АКТГ от 1000 пг на 1 мл зоны соприкосновения с одеждой, открытые участки тела, складки приобретают темно-коричневый цвет с фиолетовым оттенком.
Вторая отличительная особенность – это необычно высокая потребность в гормонах для заместительной терапии. При высоком уровне АКТГ введенные препараты быстро разрушаются. С этим связано развитие адреналовых кризов при малейшем перенапряжении или даже на фоне полного благополучия.
Криз бывает относительно легким – нарастает слабость, снижается аппетит, появляется ломота в костях, суставах, снижается давление крови. Тяжелее протекают внезапные «большие» приступы:
- выраженная тошнота, рвотные позывы;
- боль в животе, понос;
- слабость достигает такого уровня, что больной не может двигаться;
- нарастают мышечные и суставные боли;
- повышена температура до 40 градусов;
- обморочные состояния, сосудистый коллапса из-за резкого падения давления.
Осложнения болезни
Растущая вверх аденома гипофиза приводит к нарушениям зрения, выпадению боковых полей, снижению четкости предметов, бывает двусторонняя слепота. Если опухоль растет вперед по отношению к турецкому седлу, то страдает обоняние и психика, при боковом распространении отекают веки, глазное яблоко смещается кпереди, появляется односторонняя слепота и головная боль.
Прорастание нижних тканей изменяет голос (гнусавый) и затрудняет глотание. Наиболее тяжелый вариант – переход на задние части мозга. У больных обнаруживают признаки стволовых нарушений, патологические рефлексы, глотание становится почти невозможным.
Молодая женщина с болезнью Кушинга, фотография вместе с ее сестрой-близнецом (А). В этом случае была проведена двусторонняя адреналэктомия. Несколькими годами позже у пациентки развился синдром Нельсона и паралич третьего черепного нерва справа (Б и В), связанный с инфильтрацией пещеристого синуса местно инвазивной кортикотропиномой (Г). Были выполнены гипофизэкгомия и лучевая терапия, благодаря которым произошел регресс паралича третьего черепного нерва (Д). Отмечается развитая пигментация кожи при синдроме Нельсона.
Психические нарушения связаны с тем, что отмечается гормональная недостаточность даже на фоне высоких доз кортикостероидов, а в крови имеется высокая концентрация АКТГ. Немаловажно и сдавление опухолью соседних структур головного мозга. Поэтому больные с синдромом Нельсона отличаются по психоневрологическому статусу от всех остальных пациентов. У них присутствует:
- резкая слабость,
- безразличие к окружающему,
- страх смерти,
- тревожность,
- выраженная депрессия,
- неврастения,
- перепады настроения,
- плаксивость.
При кровоизлиянии в ткань опухоли появляется резкая головная боль, подает давление, возникает тошнота, рвота, нарушается двигательная активность и чувствительность.
Диагностика состояния больного
Для заболевания наиболее информативным показателем является высокая концентрация АКТГ вне зависимости от времени суток.
Обнаружить саму аденому гипофиза не всегда просто, так как кортикотропинома часто имеет маленький размер и может не изменять очертания турецкого седла. В таких случаях прибегают к увеличению рентгенографических снимков и КТ. Большая опухоль нарушает структуру своего ложа, выпрямляет, истончает или разрушает турецкое седло, углубляет его дно, повреждает костные отростки
Характерны офтальмологические изменения:
- изменения на глазном дне,
- опущение верхнего века,
- исчезновение боковых полей зрения,
- частичная или полная слепота.
Компьютерная томография головного мозга
Лечение синдрома Нельсона
Цели терапии – компенсировать дефицит кортизола, подавить образование АКТГ, предупредить последствия роста опухоли. Для этого назначают медикаменты, облучение и операцию
Медикаментозная терапия
Лекарственными средствами, которые используют для подавления образование АКТГ, являются Перитол (антиаллергический препарат, блокатор серотонина), Парлодел (стимулятор дофамина) и Депакин (Конвулекс).
Их действие проявляется не во всех случаях. Иногда удается достичь длительной ремиссии, а на часть пациентов они не действуют.
Редко используются как основной метод лечения, чаще для послеоперационной профилактики рецидивов.
Лучевая терапия
Облучение может быть проведено дистанционно гамма-лучами и протонами, а также в сам гипофиз вводится радиоактивное золото, которое постепенно разрушает опухоль. Этот способ подходит только для небольших образований, которые не выходят за пределы турецкого седла. Как и медикаменты, облучение назначают после оперативного лечения.
Операция
Если направление роста опухоли идет вниз от гипофиза, то ее лучше удалить при доступе через носовые ходы. При растущих вверх аденомах или крупных новообразованиях применяется трепанация черепа. Положительный результат от удаления чаще бывает при небольших размерах, пока нет признаков сдавления соседних тканей.
Удаление аденомы гипофиза через носовые ходы
Прогноз для больного
Последствия синдрома Нельсона зависят от быстроты роста опухоли и возможности компенсировать недостаточность надпочечников. Удовлетворительное состояние бывает при медленном прогрессировании гормональных нарушений и микроаденомах. При больших образованиях даже после удаления аденомы гипофиза не всегда удается полностью восстановить зрение и неврологический статус
Профилактика
Для того, чтобы предупредить развитие патологии после удаления надпочечников пациенты должны находиться под наблюдением эндокринолога. Особенностью синдрома Нельсона считается то, что он возникает как на протяжении 3-6 месяцев, так и через десяток лет.
Поэтому не реже, чем раз в 3 месяца нужно проходить эндокринолога, раз в полугодие – невропатолога и определять величину АКТГ, электролитный баланс, показатели жирового и белкового обмена. Томография с контрастированием назначается ежегодно.
Рекомендуем прочитать статью о недостаточности гипофиза. Из нее вы узнаете о причинах недостаточности функции гипофиза у взрослых и детей, симптомах синдрома, а также о диагностике и методах лечения недостаточности гипофиза.
А здесь подробнее о профилактике эндемического зоба.
Синдром Нельсона возникает у пациентов с двусторонней адреналэктомией. Операция проводится при болезни Иценко-Кушинга.
Так как ее причина – это аденома гипофиза, то после удаления надпочечников она активно растет и вырабатывает АКТГ. Это проявляется потемнением кожи и развитием адреналовых кризов.
Лечение – преимущественно оперативное, для профилактики рецидивов его дополняют медикаментами и лучевой терапией.
Источник: https://endokrinolog.online/sindrom-nelsona/
Синдром Нельсона
Синдром Нельсона — аденома гипофиза, активно продуцирующая кортикотропин на фоне выраженной гиперпигментации кожи, слизистых оболочек и лабильного течения манифестной надпочечниковой недостаточности.
Синдром Нельсона развивается после двухсторонней адреналэктомии. Частота развития синдрома Нельсона колеблется в широких пределах от 10 до 80%, что обусловлено вариабельностью интерпретации клинических проявлений и используемых технических диагностических средств.
Этиология и патогенез
Этиология и патогенез обусловлены прогрессированием гиперпродукции АКТГ-кортикотропиномой гипофиза, при которой исчезает суточный ритм секреции кортиколиберина-АКТГ-кортизола, отсутствует тормозящий эффект уровня кортизола на продукцию кортиколиберииа и АКТГ на фоне гормонально-активной аденомы гипофиза, развивающейся после двухсторонней адреналэктомии. При этом рецепторы кортикотрофов микроаденомы гипофиза и ядер гипоталамуса активируют автономную продукцию гормонов.
В настоящее время получены доказательства наличия генных мутаций, определяющих глюкокортикоидную резистентность, что подтверждено также наличием нарушений трансдукции глюкокортикоидного сигнала на уровне кортикотрофов.
Предрасполагающие факторы развития синдрома Нейлона:
- высокий уровень кортизола с выраженной гиперкортизолурией до хирургического лечения центрального гиперкортицизма;
- наличие микроаденомы гипофиза;
- молодой возраст на момент двухсторонней адреналэктомии.
В то же время хирургическое вмешательство на гипофизе оказывает протективный эффект в отношении развития синдрома Нельсона.
Симптомы
Клинические проявления синдрома Нельсона складываются из выраженной гиперпигментации, лабильного течения надпочечниковой недостаточности и нейроофтальмологических симптомов.
Гиперпигментация кожи и слизистых оболочек — стабильный и ранний признак синдрома Нельсона, появляется на открытых участках тела и в области складок и местах трения одеждой. Считается, что выраженность гиперпигментации коррелирует со степенью повышения уровня АКТГ.
Вторая группа симптомов — лабильность течения надпочечниковой недостаточности — связана с ускорением метаболизма кортизона и проявляется нарастанием слабости, адинамии, ухудшением аппетита, диспептическими нарушениями, болями в костях, артериальной гипотонией. Возможно развитие аддисонического криза с развернутой симптоматикой.
Нейроофтальмологические симптомы определяются размерами опухоли и направлением ее роста и характеризуются:
- упорными головными болями вследствие нарушения ликворооттока;
- снижением памяти, утомляемостью, слезливостью, снижением работоспособности, мнительностью, эмоциональной неустойчивостью;
- при антеселлярном росте возможны нарушения обоняния;
- при параселлярном росте возникают нарушения со стороны III, IV, V и VI пар черепно-мозговых нервов, т.е. нарушения полей зрения в виде битемпоральной гемианопсии или квадрианопсии, снижение остроты зрения вследствие паралича глазодвигательных нервов или первичной атрофии зрительного нерва;
- при супраселлярном росте, прорастании или сдавлении в области III желудочка появляются общемозговые симптомы.
Диагностика
Лабораторная и инструментальная диагностика синдрома Нельсона основывается на результатах исследования уровня АКТГ и подтверждения наличия микро или макроаденомы гипофиза, характеристики ее роста и оценки динамики роста аденомы в сравнении с периодом после двусторонней адреналэктомии до развития синдрома Нельсона.
Для кортикотропиномы в условиях удаленных надпочечников характерно повышение уровня АКТГ более 200 пг/мл и отсутствие циркадианного ритма секреции. Как правило, величина АКТГ отражает активность аденомы и соответствует выраженности гиперпигментации.
При быстро растущих аденомах с инфильтративным ростом и резко выраженной гиперпигментации уровень АКТГ может достигать 3000 пг/мл и более.
Лечение
Лечение направлено на достижение компенсации хронической надпочечниковой недостаточности и воздействие гипоталамо-гипофизарную систему.
Применяются различные методы, подавляющие секрецию АКТГ и предотвращающие рост и развитие кортикотропиномы — медикаментозная терапия, лучевое воздействие на гипофиз и хирургическое удаление опухоли.
Медикаментозная и лучевая терапия применяются в случаях новообразований, не выходящих за пределы турецкого седла либо в случах рецидива или частичного терапевтического эффекта после хирургического лечения.
Прогноз
Прогноз заболевания зависит от динамики развития аденомы гипофиза и степени компенсации надпочечниковой недостаточности.
При медленном развитии опухолевого процесса и компенсации надпочечниковой недостаточности состояние больных длительное время может оставаться удовлетворительным. Трудоспособность почти у всех ограничена.
Необходимо диспансерное наблюдение эндокринолога, невропатолога и окулиста.
Профилактика
Большинство авторов признают, что предупредить развитие синдрома и больших опухолей легче, чем лечить синдром Нельсона с распространенными процессами за пределами турецкого седла.
Предварительная лучевая терапия на область гипофиза больных болезнью Иценко-Кушинга, по данным большинства авторов, не предотвращает развитие синдрома.
В целях профилактики независимо от предварительного облучения гипофиза при болезни Иценко-Кушинга после двусторонней тотальной адреналэктомий необходимо ежегодно проводить рентгенографическое исследование турецкого седла, полей зрения и содержания адренокортикотропного гормона в плазме крови.
Источник: http://medicoterapia.ru/sindrom-nelsona.html
Предмет, задачи и методы патологии
Патология — фундаментальная наука, изучающая закономерности возникновения, развития и завершения болезней. Предметом ее исследования является больной организм.
Как учебная дисциплина патология основывается на синтезе двух наук: патологической физиологии и патологической анатомии.
Методы, используемые в патологии. Для познания и объяснения сущности патологических процессов и болезней патология использует данные:
- клинического обследования больных;
- морфологического изучения прижизненно взятых участков тканей больного организма;
- результаты исследования трупов;
- моделирование болезней.
Патология включает два раздела — общую и частную патологию.
Общая патология изучает типовые (стереотипные) патологические процессы, лежащие в основе болезней, — дистрофию, некроз, атрофию, нарушения крово- и лимфообращения, воспаление, аллергию, лихорадку, гипоксию, а также приспособительные и компенсаторные реакции, шок. стресс и опухоли.
- Частная патология изучает конкретные болезни, причины и механизмы их развития, проявления, осложнения и исход отдельных заболеваний.
- Патология является теорией медицины, так как именно она позволяет раскрыть сущность болезни, выявить ее функциональные и структурные проявления, указать направление поиска принципов профилактики и лечения болезней.
- Для решения стоящих перед ней задач патология использует два подхода:
- патофизиологический, который позволяет изучить расстройства в организме на разных этапах развития отдельных патологических процессов и болезней в целом:
- патоморфологический, который, с помощью разнообразных современных морфологических методов, дает возможность исследовать нарушения структуры органов и тканей во время болезни, при выздоровлении или гибели организма.
Вместе с тем единство и взаимообусловленность фикции и структуры в норме и при патологии стирают грань между этими двумя подходами, и они по существу лишь дополняют друг друга.
Так, патофизиология в настоящее время широко использует для анализа патологических процессов морфологические методы.
Патологическая анатомия в свою очередь располагает методами, позволяющими оценивать функцию поврежденных структур.
Патологическая анатомия использует несколько методов. К ним относятся биопсия, вскрытие трупов и эксперименты на животных.
Биопсия — прижизненное исследование кусочков тканей и opганов больного. Высокое техническое оснащение современной клинической медицины позволяет получить фрагмент ткани (биоптат) практически любого органа человека.
Анализируя с пoмощью микроскопа и других методов изменения, обнаруженные в биоптате, патологоанатом устанавливает прижизненный клинический диагноз заболевания.
Результаты исследования биопсийного материала позволяют выявить болезнь на самых ранних этапах ее развития, когда еще отсутствуют четкие клинические симптомы заболевания. Это дает возможность рано начать лечение и служит залогом благоприятного исхода болезни.
В ряде случаев только патологоанатом может установить правильный диагноз (например, точно определить характер опухоли).
Вскрытие (аутопсия) трупов умерших больных проводится для выяснения тех изменений в органах и тканях, которые были вызваны болезнью, а также для установления причины смерти; по результатам вскрытия составляется патологоанатомический диагноз.
Эксперименты на животных широко используются для изучения морфологических изменений в органах и тканях в процессе болезни, от самых ранних ее проявлений до завершения, а также с целью оценки эффективности различных методов лечения.
Патофизиология — фундаментальная дисциплина, и поэтому моделирование (в том числе на животных) болезней, близких к заболеваниям человека, является ее ведущим методом.
Эксперимент позволяет вскрыть сущность предболезненных состояний и самых ранних стадий заболевания, что не всегда удается в клинике.
С помощью экспериментальных моделей исследуют механизм мы развития болезней, оценивают разные способы их лечения, находят пути управления течением заболевания (экспериментальная терапия), разрабатывают проблемы диагностики и профилактики болезней.
Любое лекарственное или нелекарственное средство, прежде чем оно будет использовано в клинике, проходит испытание на животных.
История патологии
Возникновение патологии и выделение ее в качестве самостоятельной науки относятся к первой половине XIX в., когда благодаря развитию химии, биологии, физиологии, хирургии, терапии и морфологии для нее была подготовлена coответствующая основа.
Первая в России кафедра патологической анатомии и патологической физиологии была организована в 1849 г. в Московском университете известным терапевтом А. И. Полуниным.
Он пepвым понял необходимость сопоставления проявлений болезни, имевшихся при жизни больного, с изменениями, которые выявлялись при вскрытии трупов. А. И. Полунин — основоположник клинико-анатомического направления, которое стало характерной чертой отечественной медицины. Идеи А. И.
Полунина продолжали и развивали его многочисленные ученики и последователи. Среди них и создатель Московской школы патологоанатомов, автор первого в России учебника по патологической анатомии проф. М. Н. Никифоров. Учениками М. Н. Никифорова были академики А. И. Абрикосов и И. В. Давыдовский.
Развивая идеи, заложенные А. И. Полуниным и М. Н. Никифоровым, А. И. Абрикосов создал принципы отечественной патологической анатомии и внес большой вклад в разработку многих проблем общей и частной патологии. И. В.
Давыдовский доказал закономерности развития патологических процессов и болезней; ему принадлежат крупные исследования в области общей патологии, патологии военного времени. Учеником М. Н. Никифорова был профессор М. А. Скворцов — признанный основоположник детской патологической анатомии.
Преемником идей Московской школы патологоанатомов стал ученик А. И. Абрикосова — академик А. И. Струков.
С его именем связаны разработки патоморфологии туберкулеза, ревматических болезней, патологии микроциркуляции, воспаления, а также введение в патологическую анатомию новых методов исследования — гистохимии, гистоферментохимии, электронной микроскопии, придавших ей функциональную направленность.
Современный этап развития патологической анатомии характеризуется появлением молекулярной патологии, изучающей болезни на молекулярном уровне, обеспечивающим межклеточные отношения. Это направление в нашей стране возглавляет академик М. А. Пальцев.
Параллельно с патологической анатомией развивалась и патологическая «физиология. В 1849 г. тот же профессор А. И. Полунин стал основателем кафедры патологической физиологии в Московском университете.
В этот период эксперимент на животных уже прочно вошел в арсенал методов научного исследования. Фундаментом для развития патологической физиологии явились исследования физиологов И. М. Сеченова, И. П. Павлова, Н. Е.
Введенского, терапевта С.П. Боткина.
В создании кафедр общей и экспериментальной патологии (патологической физиологии) в России большая заслуга принадлежит выдающемуся физиологу, ученику И. М. Сеченова — проф. В. В. Пашутину. Его научные исследования были сосредоточены на механизмах нарушения обмена веществ, голодании и патологии эндокринной системы.
Крупный вклад в развитие общей патологии внесли отечественные патофизиологи профессора А.Б. Фохт, А.А. Богомолец, Н.Н. Аничков, С.С. Халатов, А.Д. Сперанский, Н.Н. Сиротинин. которые разрабатывали различные аспекты проблем реактивности, старения, патологии эндокринной системы. Н. Н. Аничков и С. С.
Халатов создали первую экспериментальную модель атеросклероза и многое сделали для понимания механизмов его развития.
Большой вклад в развитие патологии внесли крупные зарубежные физиологи и морфологи — К. Бернар. В. Кеннон. К. Рокитанский, Р. Вирхов, Г. Селье. Так, известный физиолог XIX века К.
Бернар является основоположником экспериментально-физиологического направления в патологии и учения о постоянстве внутренней среды организма — гомеостазе. Крупнейший немецкий патолог Р. Вирхов — основатель учения о клеточной патологии.
Клеточная теория патологии стала мощным стимулом для изучения и систематизации клеточных, а позднее субклеточных механизмов развития болезни. Широкую известность и pacпpoстранение получили исследования Г.
Селье, показавшего важную роль нейроэндокринной системы в формировании приспособив тельных реакций и расстройств жизнедеятельности. Он является основоположником учения о стрессе.
В настоящее время патология имеет в своем арсенале большой комплекс современных физиологических и морфологических методов исследования. Изучение патологических процессов и болезней проводится на организменном, органном, клеточном, cyбклеточном и молекулярном уровнях.
Использование современных методических подходов позволило вскрыть ряд важных для медицины общебиологических закономерностей.
Основополагающие ми среди них являются представление о типовых, или стереотипных, реакциях; учение о гомеостазе; представление о том, что в основе всех патологических процессов лежат физиологические реакции; гетерогенность.
Представление о типовых, или стереотипных, реакциях, т. е. об относительно небольшом наборе ответов организма на изменения окружающего мира и внутренней среды, распространяется на все и физиологические, и патологические процессы.
Стереотипные реакции проявляются на всех уровнях организации живой материи.
На молекулярном уровне набор стереотипных реакций относительно невелик, на уровне внутриклеточных структур их несколько больше (например, в митохондриях могут происходить набухание, потеря матрикса, разрушение крист, разрыв наружной мембраны); на уровне клетки — секвестрация (отделение части клетки), дифференцировка, деление, созревание. Различные сочетания стереотипных реакций на уровне внутриклеточных структур, клеток, тканей и органов в условиях патологии составляют специфику общепатологических процессов, а на уровне систем и всего организма — картину болезни.
Учение о гомеостазе — совокупности типовых реакций, составляющих относительное постоянство состава крови, метаболизма, температуры тела, артериального давления, иными словами — постоянства внутренней среды. Эти же реакции определяют ответы организма на патогенные воздействия.
В основе всех патологических процессов лежат физиологические реакции, и никаких других, особых реакций, появляющихся только при развитии патологии, не существует.Ответные реакции организма на действие раздражителя в пределах параметров гомеостаза являются нормальными, физиологическими.
Но если в ответ на действие раздражителя нарушаются структурно-функциональные основы гомеостаза, те же самые реакции становятся патологическими. Они могут вызвать гибель не только отдельных частей организма, но и его смерть.
Так, способность крови свертываться в норме — действительно защитная физиологическая реакция, предупреждающая смерть от кровотечения при повреждениях. Но та же реакция в определенных неблагоприятных условиях приводит к образованию тромба, закрывающего просвет coсуда, что вызывает повреждение тканей организма (например, инфаркт миокарда).
Воспалительный процесс в норме направлен на защиту организма от патогенных раздражителей, но при oпpeделенных условиях он может вызвать летальный (смертельный) исход.
Гетерогенность — еще одна важная биологическая закономерность. Органы функционируют на протяжении многих десятков лет потому, что в каждый данный момент функционально активна не вся ткань органа, а только ее определенная часть.
Функционирующие структуры разрушаются, для их восстановления требуются время, энергетические и пластические затраты. Пока идет процесс восстановления разрушившихся структур, функция органа осуществляется другими структурами, которые в свою очередь тоже разрушаются.
Все это в норме создает структурнофункциональную мозаичность органов и тканей, которая называется гетерогенностью. Она выявляется на всех уровнях жизнедеятельности: даже отдельная митохондрия не функционирует в клетке одновременно всей своей структурой.
Явление гетерогенности создает функциональный (жизненный) резерв организма. Исчезновение гетерогенности структур клеток и тканей является плохим прогностическим признаком, указывающим на истощение резервных возможностей организма.
Знание указанных биологических закономерностей позволяет правильно понять болезнь, оценить состояние больного и проводить целенаправленное лечение.
Источник: https://auno.kz/patologiya/254-predmet-zadachi-i-metody-patologii.html